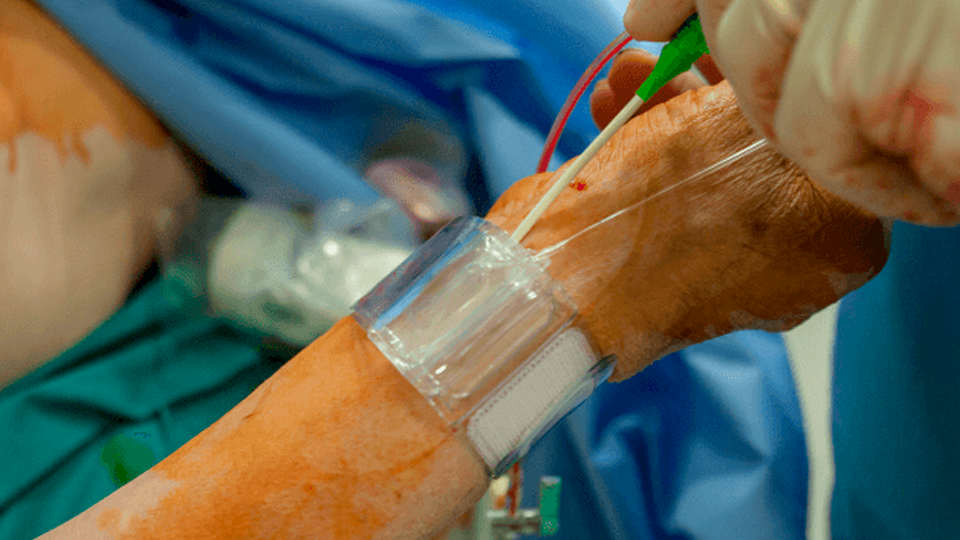
19 de Enero de 2026. Un reciente estudio internacional ha revelado datos clave para mejorar la seguridad en los procedimientos del corazón. En la cardiología intervencionista moderna, los médicos suelen ingresar a las arterias a través de la muñeca (acceso radial) para realizar diagnósticos y tratamientos, pero siempre ha existido el debate sobre qué brazo es más conveniente. Este nuevo análisis, que incluyó a más de 9,400 pacientes hasta mediados de 2025, demuestra que utilizar el brazo izquierdo reduce significativamente la exposición a la radiación tanto para la persona atendida como para el equipo médico que realiza la intervención.
La investigación determinó que, al usar el acceso izquierdo, el tiempo de uso de los rayos X es más corto y la dosis total de radiación recibida por el paciente es menor en comparación con el brazo derecho. Esto se debe a que la ruta desde el brazo izquierdo suele ser más directa hacia el corazón, lo que facilita el movimiento de los instrumentos médicos y hace que el procedimiento sea más ágil. Al reducir el tiempo de trabajo, se optimiza el uso de los equipos y se minimizan los riesgos asociados a la energía radiológica.
Para los especialistas, los beneficios son igualmente importantes, ya que el estudio confirmó que los médicos reciben una carga de radiación significativamente menor en su cuerpo cuando operan desde el lado izquierdo. Estos hallazgos son fundamentales para los centros de salud que buscan elevar sus estándares de seguridad ocupacional y ofrecer una atención de vanguardia. Contar con los insumos adecuados para este tipo de abordajes es el siguiente paso para convertir esta evidencia científica en una ventaja real dentro de la sala de operaciones.

